 |
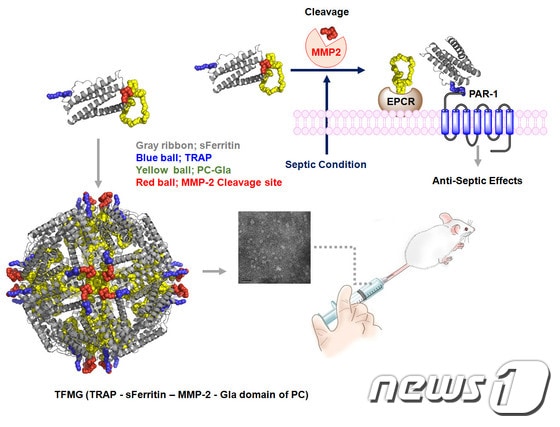
| 혈관내피세포의 수용체를 활성화시켜 세포보호작용을 나타내는 나노약물전달체 (TFMG)의 개념도.© News1 |
미래창조과학부와 한국연구재단은 7일 경북대 배종섭 교수, KIST 김인산 박사 공동연구팀이 '나노 약물전달체'를 개발했다고 밝혔다.연구팀에 따르면 이 전달체는 혈관 내피세포의 세포막 보호 및 항염증 효과를 활성화시키는 수용체*에 약물을 효율적으로 전달할 수 있다.
기존 패혈증 치료제 자이그리스®(Activated Protein C, 이하 APC**)는 정상적인 혈액 응고를 방해하는 부작용과 약물 주사 후 효능이 반으로 줄어드는 시간이 지나치게 짧다는 단점 등이 있었다.
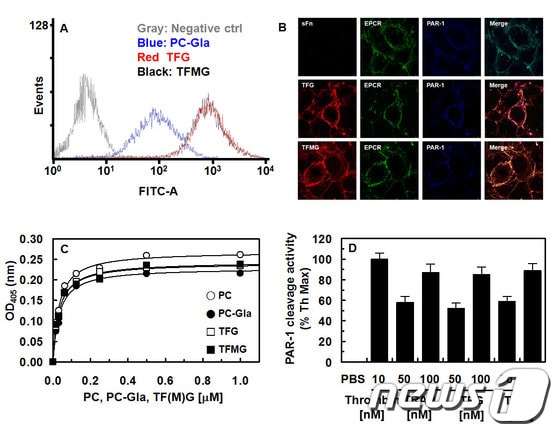 |
| 나노약물전달체 (TFMG)의 결합력 확인.© News1 |
이를 통해, PC-Gla 및 TRAP를 보다 효율적으로 수용체(EPCR, PAR-1)를 활성화, APC의 항응고 부작용을 해결함과 동시에 31분 정도이던 짧은 반감기를 5시간43분으로 10배 이상 향상시켜 효능을 개선했다.
배 교수는 "살인진드기, 에볼라 그리고 메르스 바이러스로 인한 사망 원인이 패혈증으로 밝혀졌으나 현재 공인된 치료제가 없는 실정"이라고 밝혔다.
그러면서 "이번 연구로 만들어진 약물을 토대로 향후 추가적인 실험 및 임상시험이 이뤄져 새로운 패혈증 치료제가 개발되길 바란다"고 덧붙였다.
 |
| 경북대 배종섭 교수(왼쪽), KIST 김인산 박사.© News1 |
연구 결과는 재료분야의 권위 있는 학술지인 어드밴스드 머티리얼즈(Advanced Materials) 온라인 판에 9월29일 게재됐다.
* 수용체 : 세포 밖에서의 자극을 인식, 세포에 특정한 반응을 일으키는 단백질 구조체.
** APC는 EPCR과 PAR-1(Protease activated receptor-1)을 활성화시켜 세포 보호 작용, 항염증 작용 등을 나타내는 물질. 자이그리스는 APC를 상품화한 제품.
*** 페리틴(Ferritin): 나노크기의 다른 치료약물 전달체보다 안정적이고 체내 면역반응도 작으며, 유전적, 화학적인 변화가 용이한 내인성 물질.
**** PC-Gla: 기존 치료제 APC에서 혈관내피세포 단백질 C 수용체(EPCR)를 활성화시키는 부위.
*****TRAP(Thrombin Receptor agonist Peptide) : PAR-1을 활성화시키는 부위.
etouch84@news1.kr










!['여고추리반3' 임수정 PD "박지윤, 달라진 모습…무서울 때 앞장서"[N인터뷰]①](https://image.news1.kr/system/photos/2024/5/20/6658927/no_water.jpg/dims/resize/276/crop/276x184/thumbnail/138x92!/optimize)
!['범죄도시4' 누적 1071만 ↑…전편 '범죄도시3' 흥행 넘어섰다 [Nbox]](https://image.news1.kr/system/photos/2024/5/21/6659836/no_water.jpg/dims/resize/276/crop/276x184/thumbnail/138x92!/optimize)
![장다아, 동생 장원영과 닮은 듯 다른 얼굴 [N화보]](https://image.news1.kr/system/photos/2024/5/21/6659963/no_water.jpg/dims/resize/276/crop/276x184/thumbnail/138x92!/optimize)







