
아스트라제네카, 美FDA 코로나백신 승인신청 철회
- 최서윤 기자
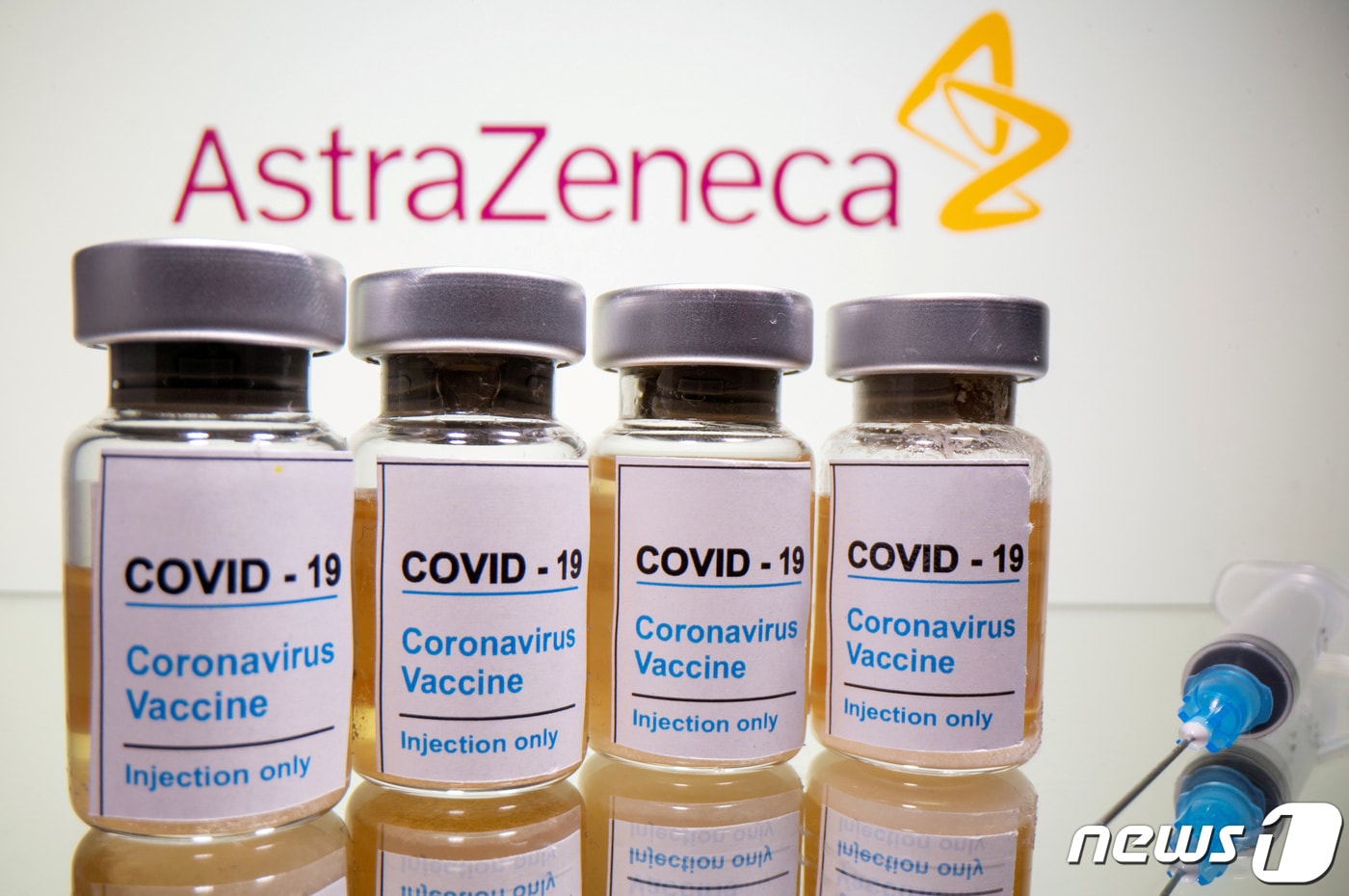
(서울=뉴스1) 최서윤 기자 = 영국 제약사 아스트라제네카는 10일 미국 식품의약품안전청(FDA)에 낸 코로나19 백신 승인을 철회한다고 10일 로이터 통신이 보도했다.
보도에 따르면 파스칼 소리오트 아스트라제네카 상임이사는 이날 한 회의에서 "더 이상 미국 승인을 기다리지 않겠다"며 이같이 밝혔다.
그는 "미국 내 백신 수요는 이제 줄고 있고 시장은 메신저리보핵산(mRNA)으로 잘 돌아가고 있다"고 덧붙였다.
옥스퍼드대가 공동개발한 아스트라제네카 코로나19 백신은 코로나 백신 개발 초기인 2020년 봄부터 미국 시장 승인 신청을 했지만 아직 받아들여지지 않았다. 미국에서는 미국 제약사 모더나, 화이자 그리고 존슨앤드존슨 자회사 얀센 제품이 승인됐다.
아스트라제네카 백신은 2020년 12월 영국에서 한 90대 여성이 접종, 세계 최초 코로나19 백신 접종 사례로 관심을 모았지만 이내 모더나, 화이자의 최신 기술을 적용한 mRNA 백신 인기에 가려졌다.
아스트라제네카가 '바이럴 벡터' 백신으로 2~8도 정도의 일반냉장상태에서도 유통이 가능한 특징을 갖는 반면, 모더나와 화이자 백신은 mRNA를 활용하며 영하 20~80도의 초저온 냉동상태에서 보관·유통을 필요로 한다.
다만 아스트라제네카 백신은 기존의 일반 백신 기술을 활용한 데다 유통 과정도 용이해 개발도상국과 저개발국 백신 공급 확대에 크게 기여한 성과도 있다.
sabi@news1.kr
Copyright ⓒ 뉴스1. All rights reserved. 무단 전재 및 재배포, AI학습 이용금지.









